南开大学李福军JACS:原子钌锚定的金属有机框架助力锂-氧电池反应动力学
文章信息
第一作者:吕清良,朱卓
通讯作者:李福军
通讯单位:南开大学
研究背景
非质子锂-氧气电池是一种具有发展潜力的储能技术,理论能量密度高达3600 Wh kg-1。然而,正极缓慢的反应动力学导致高充放电过电压和较低的能量效率。绝缘的环状Li2O2产物易堵塞正极孔道,与正极活性位点接触有限,致使Li2O2分解困难,进而导致电池容量衰减,循环稳定性较差。因此,亟需设计高效正极催化剂以调控放电产物Li2O2形成过程及形态、降低Li2O2/正极的界面阻抗,进一步提高Li2O2的分解动力学。
Li2O2的生长动力学与反应中间体LiO2在正极表面的吸附强度有关,这主要取决于放电电流密度、电解质和阴极催化剂等。科研人员尝试通过调控正极催化剂表面电子结构以调节正极反应过程,最终改变Li2O2生长形态。特定暴露晶面的RuO2, Co9S8和MnO2催化剂表现出较强的LiO2亲和力,诱导形成膜状Li2O2并改善充电反应动力学。然而,它们的低催化选择性导致电池发生副反应,充放电过电压始终高于1.0 V,循环稳定性较差。导电金属有机框架材料(c-MOFs)因其均匀分散的活性中心、开放的多孔结构和可调节的孔径在氧还原/氧析出反应等领域引起了广泛的研究。MOFs可通过选择性地改变金属节点来调节电子结构,并提供原子尺度视角来理解催化活性和结构特性之间的关系。因此,设计开发c-MOFs催化剂改变锂-氧气电池正极反应路径并调节Li2O2的沉积形态是非常有希望的。
成果简介
近日,南开大学李福军研究员团队在Journal of the American Chemical Society期刊上发表题为“Atomic Ruthenium Riveted Metal-Organic Framework with Tunable d-Band Modulates Oxygen Redox for Lithium-Oxygen Batteries”的研究性论文。本文利用离子交换策略将Ru原子锚定在具有Ni-N4位点的导电金属有机框架(Ni-HTP)骨架上,形成NiRu-HTP纳米线阵列。原子分散Ru-N4位点的引入改变了c-MOF的活性中心,引起费米能级附近的电子发生自旋极化并显著提升d轨道能级,进而对LiO2中间体表现出很强的吸附力,使其在NiRu-HTP周围发生聚集,从而产生较高的局部浓度。LiO2在NiRu-HTP表面歧化转化,形成薄膜状Li2O2,加速电荷转移并穿过正极/电解质界面,促进其在充电过程中可逆地分解。NiRu-HTP正极在锂-氧气电池中具有0.88 V的低充放电过电压,并展现出优异的循环稳定性。这项工作丰富了调控氧电催化动力学的设计理念,并为锂-氧气电池的发展提供了新的思路。
图文解析
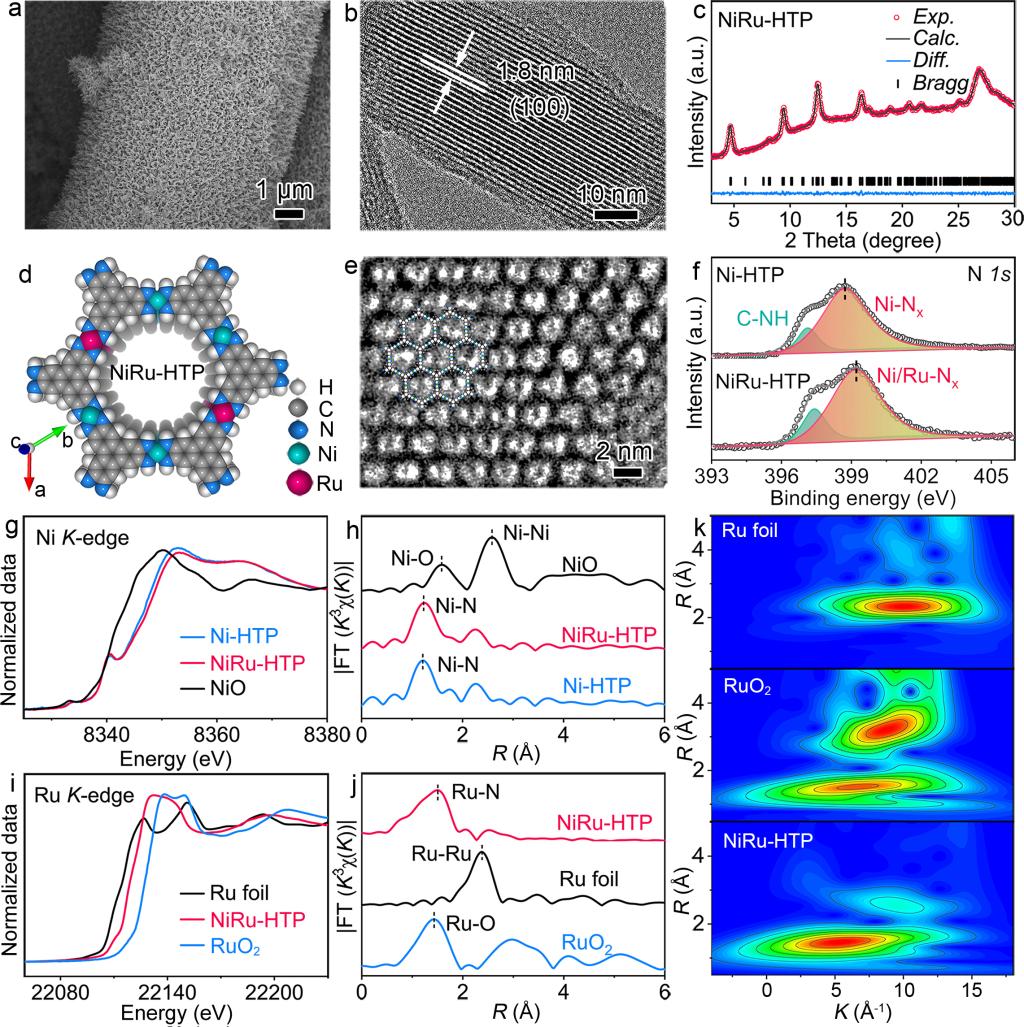
图1. NiRu-HTP的(a)SEM图像;(b)TEM图像;(c)Pawley精修谱图;(d)c轴方向的结构模拟图;(e)HRTEM图像;(f)NiRu-HTP和Ni-HTP的N 1s谱图;(g-j)Ni和Ru的XANES与XANES光谱;(k)Ru的小波分析。
要点:
1. NiRu-HTP纳米线阵列在碳纤维上的径向生长增大了比表面积,有利于催化活性位点的暴露,加速电子转移及离子扩散。
2. NiRu-HTP中的Ni和Ru原子分别与两个去质子化的HTP配体配位形成原子分散Ni-N4与Ru-N4位点,完成平面四边形配位结构并在二维方向扩展形成类层状石墨烯结构。

图2.(a, b)Ni-HTP和NiRu-HTP计算的PDOS;(c-f)Ni-N4和Ru-N4位点分别与吸附的O2分子间相互作用的PDOS及差分电荷密度分析。
要点:
1. 原子Ru在Ni-HTP的锚定引起费米能级附近的电子发生自旋极化,显著提高金属位点的d轨道能级并增强Ni-HTP导电性。
2. 相比于Ni-N4,Ru-N4位点的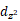 和
和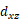 轨道与O2的σ和π轨道杂化后分别形成低电子占据及更高能级的(
轨道与O2的σ和π轨道杂化后分别形成低电子占据及更高能级的(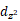 -σ)*和(
-σ)*和(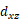 -π)*轨道,加速电子转移并促进Ru-O2的相互作用,显著增强O2的吸附及活化能力。
-π)*轨道,加速电子转移并促进Ru-O2的相互作用,显著增强O2的吸附及活化能力。
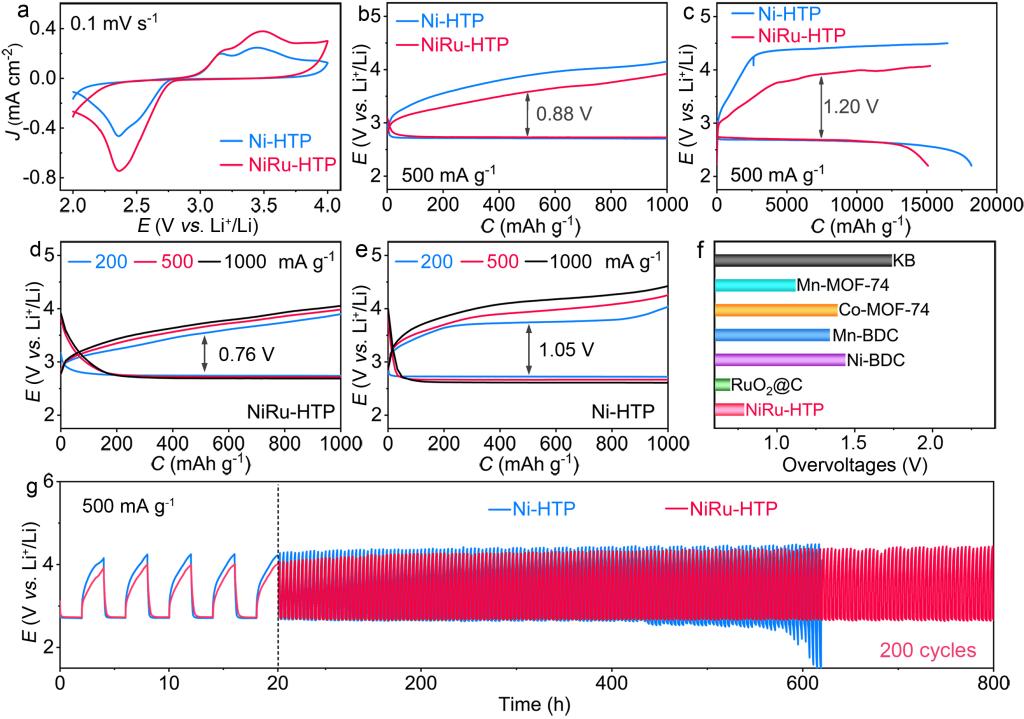
图3.(a)CV曲线;(b-e)500 mA g-1时Li-O2电池的初始充电/放电曲线、完全充电/放电曲线及电池的倍率性能;(f)NiRu-HTP与已报道的电催化剂在200 mA g-1时的放电/充电过电压的比较;(g)500 mA g-1下的长循环充/放电曲线。
要点:
1. Ni-HTP和NiRu-HTP正极在还原过程中显示出两个还原峰,分别对应LiO2及Li2O2的逐步形成。在氧化过程中明显的两个氧化峰归因于以LiO2中间体及Li2O2的分解。
2. 相比于Ni-HTP,NiRu-HTP正极在锂-氧气电池中具有更高的ORR/OER催化活性,电池充放电过电压低至0.88 V,并展现出优异的倍率及循环性能。
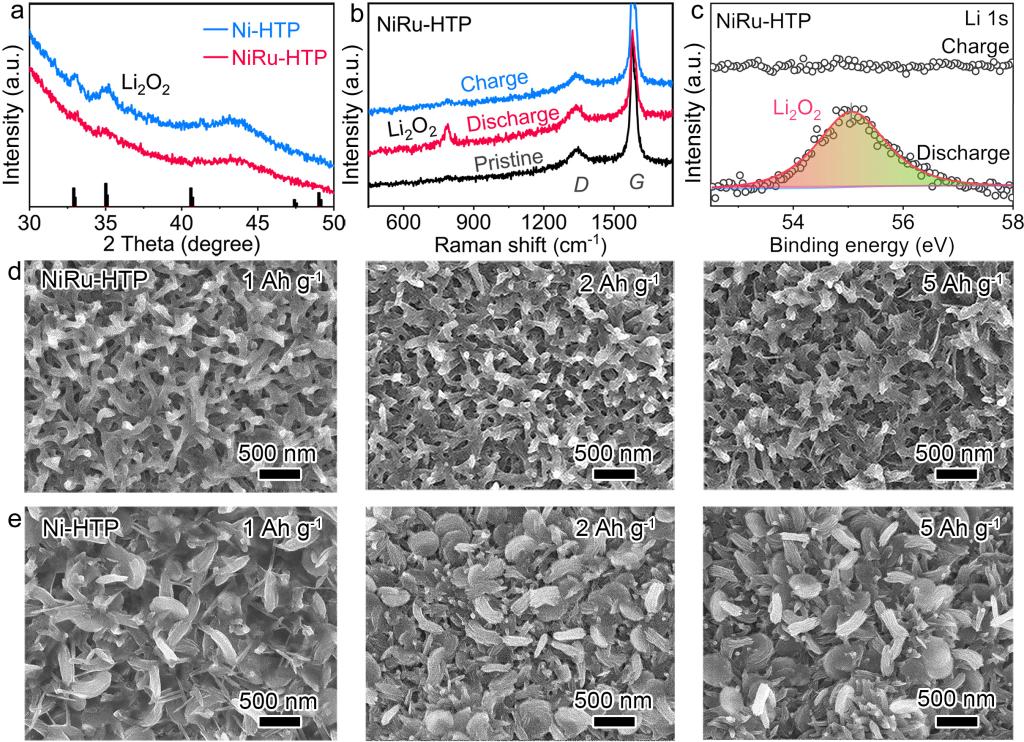
图4.(a)NiRu-HTP放电和充电后的XRD谱图;(b, c)拉曼光谱和Li 1s XPS光谱;(d, e)500mA g-1时正极截止容量分别为1, 2和5 Ah g-1的SEM图像。
要点:
1. 在放电过程中,Ni-HTP电极随着放电容量的增加产生更多环状Li2O2颗粒覆盖在电极表面,而在具有Ru-N4位点的NiRu-HTP电极上产生了一种独特的膜状Li2O2,并随着容量的增加,膜状的Li2O2逐渐填充在纳米线空隙中,这有利于电荷转移并穿过NiRu-HTP正极极/电解质界面,加速Li2O2的分解并降低充电过电压。
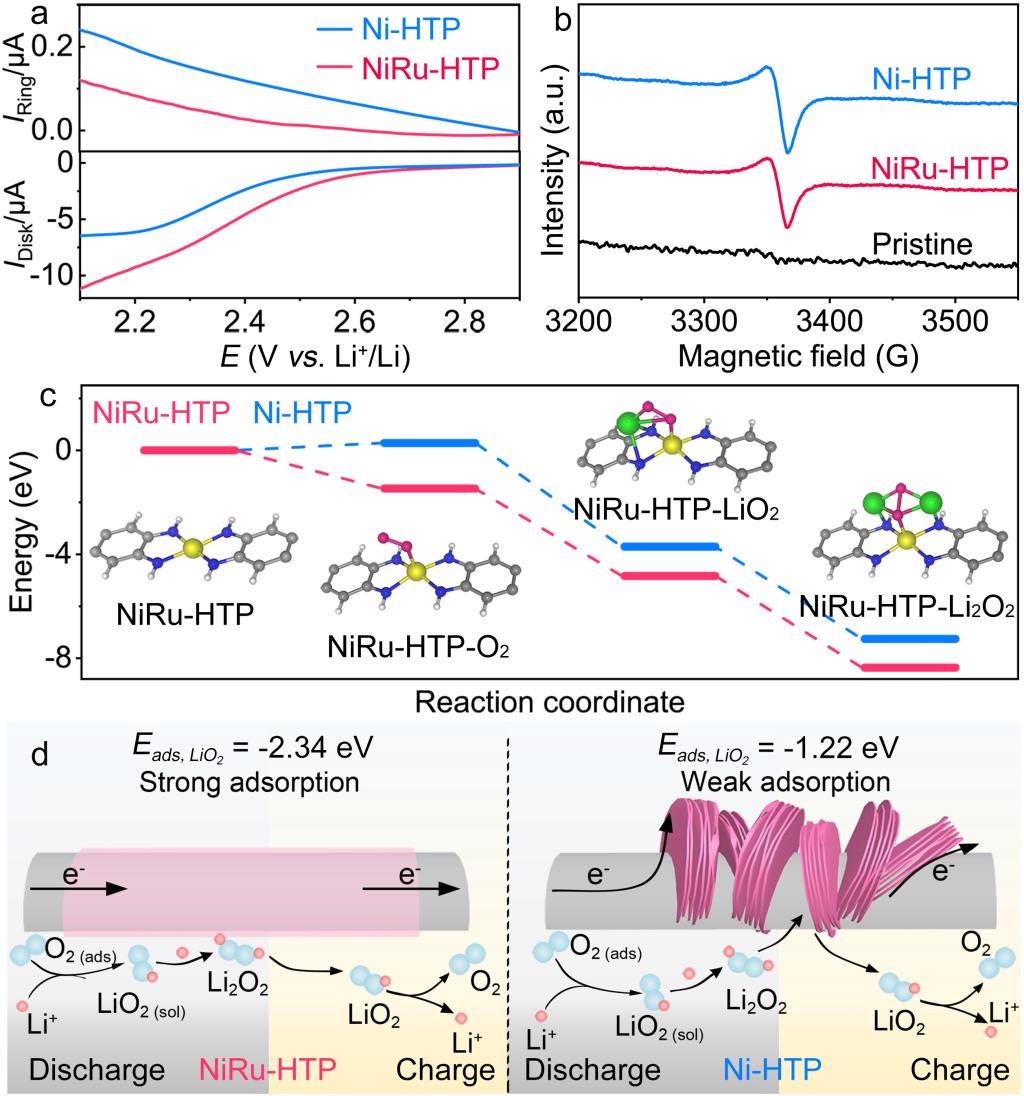
图5.(a)在O2饱和的1.0 M LiTFSI/G4电解质中测试的RRDE曲线图;(b)Li-O2电池放电后电解质的EPR光谱;(c)放电反应自由能图;(d)电池的反应机制。
要点:
1. 电池放电过程中,O2首先经历单电子还原生成LiO2中间体。在NiRu-HTP中,原子分散的Ru-N4位点对LiO2具有较强吸附性并促使其在纳米线阵列周围聚集,从而使局部浓度升高,最终形成致密的膜状Li2O2,有利于充电反应的电荷转移和离子扩散,加速其分解动力学。而Ni-HTP上Ni-N4位点对LiO2中间体吸附较弱,LiO2会溶解到电解质中经历歧化或二次还原生成环状Li2O2。由于大尺寸环状颗粒远离催化活性表面,导致产生较高的充电极化。这表明Li2O2的生长动力学与正极催化剂的表面性质有关,其决定了电池的界面反应动力学和可逆性。
文章链接
Qingliang Lv‡ Zhuo Zhu‡ Youxuan Ni, Bo Wen, Zhuoliang Jiang, Hengyi Fang, and Fujun Li*. Atomic Ruthenium Riveted Metal-Organic Framework with Tunable d-Band Modulates Oxygen Redox for Lithium-Oxygen Batteries, Journal of the American Chemical Society 2022.
 先进能源材料化学教育部重点实验室(南开大学)
Key Laboratory of Advanced Energy Materials Chemistry, Ministry of Education (Nankai University)
先进能源材料化学教育部重点实验室(南开大学)
Key Laboratory of Advanced Energy Materials Chemistry, Ministry of Education (Nankai University)
