成果简介
近日,南开大学程方益研究员(通讯作者)等人报道了一种通过在铜催化剂上修饰冠醚的策略用于提高酸性条件下二氧化碳甲烷化反应的碳利用率和选择性。
研究表明大环18-Crown-6能够富集铜电极表面附近的钾阳离子,同时增强界面电场以稳定*CO中间体,并加速水解离以促进*CO质子化。在pH=2的电解液中,18-Crown-6和铜纳米粒子的混合物对CO2电还原反应的CH4法拉第效率达到51.2%,单程碳效率为4.3%。
这项研究提供了一种简便的策略,通过使用超分子修饰Cu催化剂来提高甲烷的选择性和碳的利用率。
研究背景
在碱性或中性环境条件下进行电催化二氧化碳还原反应(CO2RR),(双)碳酸盐的自发生成不仅降低了碳的利用率(理论上 CO2RR 与 CH4 的最大比率为 20%),而且还降低了 CO2RR 技术的总能效,因为 CO2 回收过程需要消耗大量能源。在酸性电解质中进行 CO2RR 是减少 CO2 损失的一个可行选择。在酸性电解质中,CO2RR 活性按照 Li+< Na+< K+<Cs+的顺序增加。
然而,在酸性介质中进行 CO2RR 所面临的挑战在于不需要但在动力学上更有利的析氢反应 (HER)。先前的研究表明二氧化碳甲烷化的关键在于同步稳定 *CO 和质子化。电极附近较高的 K+分布可增强电场以稳定*CO,而与 H2O 形成氢键的分子则可以促进质子(*H)的传输。
图文导读
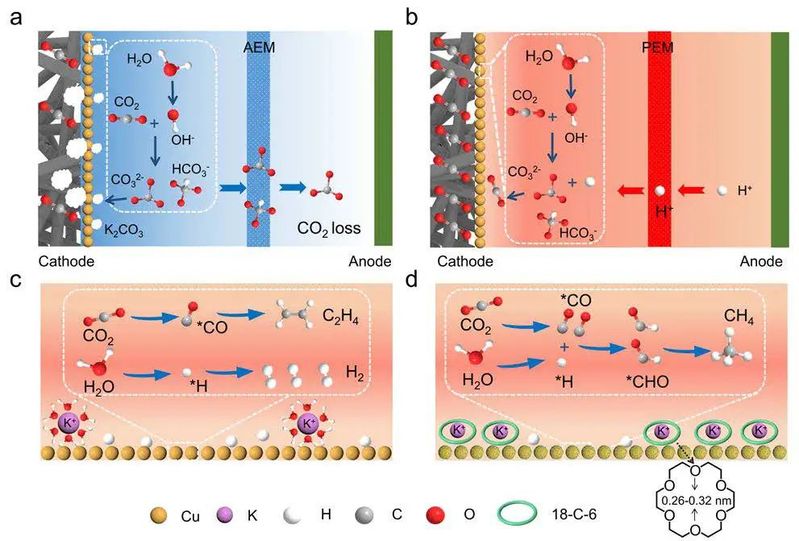
图1. AEM和PEM来分离碱性和酸性电解质中的CO2RR的差异。在酸性条件下进行CO2RR反应时,不含或含有18-C-6分子的影响。
在没有 18-C-6 的情况下,质子会与 K+ 竞争性地吸附在电极界面上,寄生 HER 占主导地位。然而,更多的 K+ 会被 18-C-6 捕获,质子在催化剂附近受阻。因此,经 18-C-6 修饰的铜电极有助于稳定更多的*CO 中间体,并促进*CO 加氢以生成 CH4。
作者首先采用超声的方法制备了18-C-6修饰铜催化剂。将商用 Cu NPs 和 18-C-6 混合在一起,催化剂用 Cu-x 表示(x 代表 18-C-6 与 Cu 的质量比)。能量色散光谱(EDS)结果表明,与原始铜催化剂相比,Cu-3 催化剂的 K+ 比例更高。电感耦合等离子体优化发射光谱(ICP-OES)测试进一步量化了 Cu-3 催化剂的 K+ 浓度是裸铜催化剂的 3.95 倍。
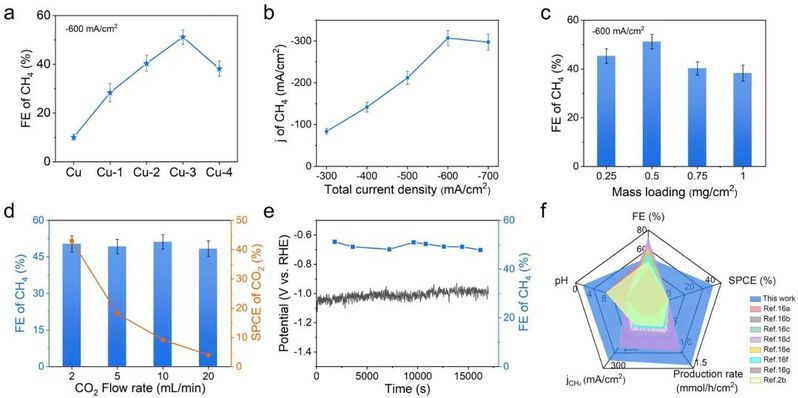
图2. 电催化性能测试。
作者使用 0.5 M K2SO4 和 H2SO4(电解液 pH 值调整为 2)的混合物作为电解液,在流动池中评估了 Cu 和 Cu-x 催化剂的 CO2RR 活性。对于 Cu-3催化剂,其在 -600 mA/cm2 时达到最高的CH4 FE 和局部电流密度 (j),分别为 51.2% 和 -307.14 mA/cm2。该值是未改性 Cu 催化剂的 ~5.1 倍。此外,作者发现随着催化剂负载量的增加,CH4 的 FE 呈现出火山式变化,其中,当催化剂载量为 0.5 mg/cm2时,CH4的FE最优。
为了评估二氧化碳的利用效率,作者测定了不同二氧化碳流速下 Cu-3 催化剂的单程碳效率 (SPCE)。当流速降低到 2 mL/min 时,CO2 的 SPCE 增加到 43.0%,而相应的 CH4 的 FE 为 50.4%。此外,在 -600 mA/cm2 下电解 16000 秒后,催化剂表现出相当高的稳定性,CH4 FE 保持在 47.9% 左右。与其他已报道的催化剂相比,Cu-3 催化剂在酸性介质中具有较高的二氧化碳利用效率、电流密度和 CH4 产率,在碱性和中性条件下也有明显的优势。
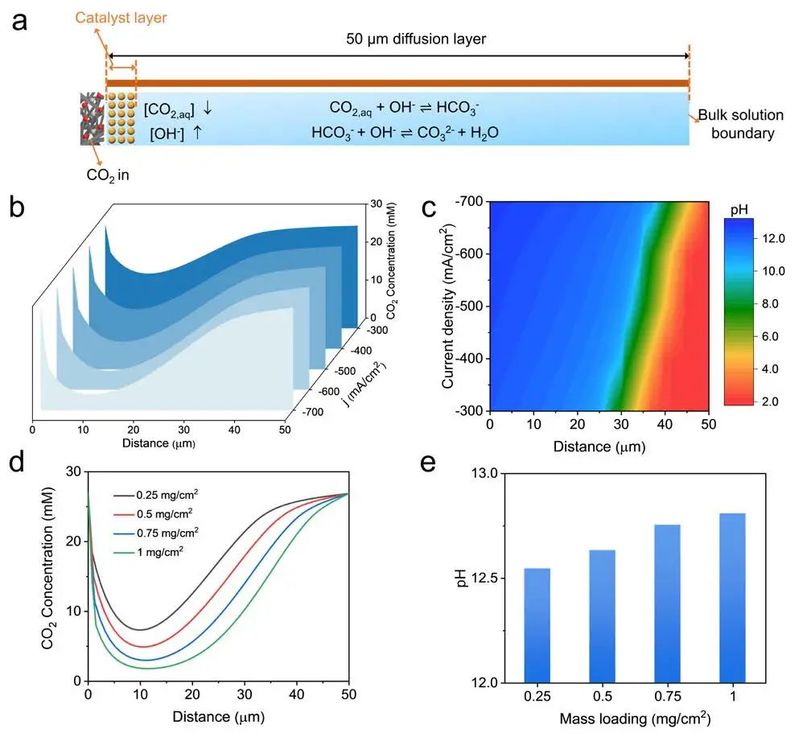
图3. 铜离子在 Cu-Cl 电解质中的氧化还原机制。
作者进一步通过有限元法模拟了阴极催化剂表面附近的局部物种和 pH 分布,以揭示 CO2RR过程中局部微环境的变化。作者综合考虑了电化学反应、物种迁移和碳酸盐平衡等各种因素建立了一维(1D)反应-扩散模型。随后,作者模拟了电流密度-300至-700 mA/cm2 时 Cu-3 表面的二氧化碳浓度和 pH 值分布。随着外加电流密度的升高,二氧化碳浓度下降得更快,最小值位置离电极表面更远。从体相电解液到电极附近的局部 pH 值会增加,电流越大,pH 值变化越快。
特别值得注意的是,酸性电解液在电极附近变为碱性,在距离表面 40 μm 的范围内,pH 值接近 8 以上。此外,作者还研究了不同质量负载催化剂的局部二氧化碳浓度和 pH 值。随着催化剂载量的增加,排出的 CO2 也逐渐增多, 由于催化剂层更厚,扩散距离更长。同时,催化剂越多,电极表面的局部 pH 值越高。
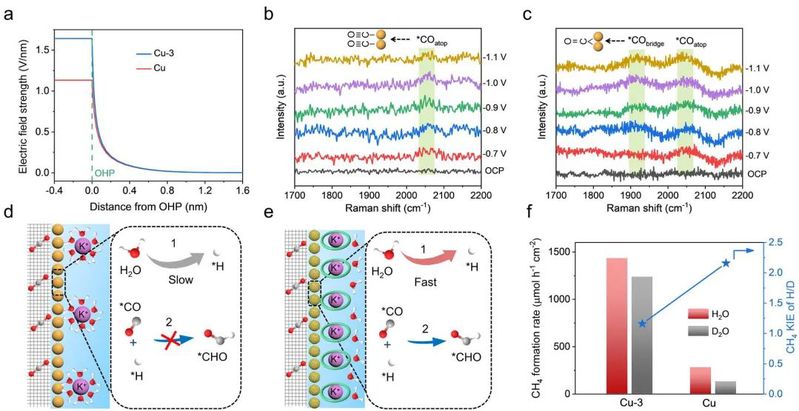
图4. 机理研究。
作者进一步通过使用含 18-C-6 和不含 18-C-6 的模型同时测量电场强度,进一步研究了电化学双层膜的特性。在纯铜电极上,水合 K+ 和质子竞争性地占据了 OHP。相比之下,K+ 被 18-C-6 配位,因此残留在 Cu-3 催化剂表面的 H3O+ 较少。由于富集了 K+,Cu-3 上的模拟电场强度高于 Cu 上的模拟电场强度。作者随后进行了原位拉曼光谱分析,以跟踪电极表面的中间产物。在Cu 电极上只观察位于∼2050 cm-1处的*COtop振动。与此相反,Cu-3 催化剂上有两个明显的带,分别表示 *COatop 和 *CObridge(位于 ∼1900 cm-1)。因此,*CO 中间体在 Cu-3 表面得到了更有效的稳定,有利于进一步质子化形成 CH4。
一般来说,*CO 质子化形成*CHO 中间体被认为是 CO2 电解甲烷化的决速步(RDS)。由于阴极表面的局部环境转变为碱性,活性 *H 应该来自水的解离,而水的解离在碱性环境中会受到阻碍。H2O 解离生成 *H 以及随后 *CO 质子化为 *CHO 中间产物的过程在具有局部碱度的纯铜上是缓慢的,而在18-C-6 分子存在的情况下则得到了加强,从而提高了甲烷化的动力学和选择性。为了验证上述假设,作者对 Cu 和 Cu-3 催化剂上的 H2O/D2O 进行了动力学同位素效应(KIE)测量。Cu 上的 CH4 生成率显著下降,测得的 KIE 为 2.16。相反,Cu-3 催化剂在 H2O 和 D2O 中的 CH4 生成率很接近,因此 KIE 值低得多,仅为 1.16,这表明质子转移过程不是一个决速步。以上结果表明冠醚修饰可促进水的解离,从而为 CO2 电甲烷化提供必要的 *H。
文献信息
Xu, Keqiang, Li, Jinhan, Liu, Fangming, Chen, Xijie, Zhao, Tete, Cheng, Fangyi, Favoring CO Intermediate Stabilization and Protonation by Crown Ether for CO2 Electromethanation in Acidic Media. Angew. Chem. Int. Ed. 2023, e202311968.
https://doi.org/10.1002/anie.202311968
 先进能源材料化学教育部重点实验室(南开大学)
Key Laboratory of Advanced Energy Materials Chemistry, Ministry of Education (Nankai University)
先进能源材料化学教育部重点实验室(南开大学)
Key Laboratory of Advanced Energy Materials Chemistry, Ministry of Education (Nankai University)
